Silikatstruktur und isomorpher Ersatz
Grundbauelemente der Silikate sind
Si-O Tetraeder sowie Al-OH-Oktaeder. Bei den Si-O Tetraedern fungiert das
4-wertige Silizium als Zentralion, das von 4 Sauerstoffatomen umgeben ist, die
tretraedrisch um das Si angeordnet sind. Bei den Al-OH-Oktaedern sind 6
OH-Ionen in Form eines Oktaederes um ein Al Zentralion angeordnet.
Die
[SiO4]4--Tetraeder können in
Silikaten isoliert vorliegen. Sie können aber auch über die Ecken der Tetraeder
zu größeren Einheiten verknüpft werden, so dass ein Sauerstoffatom jeweils zwei
Tetraedern angehört. Die Tetraeder werden nicht über die Kanten oder Flächen
mitenander verknüpft. Die so entstandenen Einheiten werden zur systematischen
Einteilung der Silikate herangezogen.
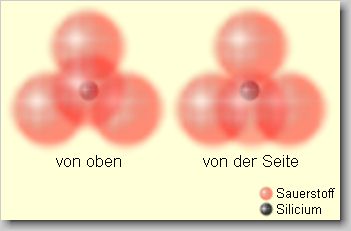 |
| Modellhafte Darstellung von zwei Ansichten (von oben und
von der Seite) einer dichten Sauerstoff-Kugelpackung, in dessen Lücke ein
Siliziumatom plaziert ist. Der Abstand Si-O beträgt ca. 1,63 ±
0,03Å. |
| (
Quelle: Büro für angewandte Mineralogie, Dr. Stephan Rudolph,
http://www.a-m.de/deutsch/lexikon/mineral/sio4-tetraeder.htm) |
Beim isomorphen Ersatz werden Kationen
mit vergleichbarem Ionendurchmesser, jedoch abweichender Ladung ausgetauscht:
In Si-Tetraedern wird das Zentralion ersetzt durch
Al3+ oder Fe3+. In
Al-Oktaedern wird das Zentralion ersetzt durch Mg3+
oder Fe2+ oder Mn2-.
Dadurch ändert sich die Nettoladung, es entsteht ein
negativer Ladungsüberschuss, der ausgeglichen wird durch die Anlagerung von
Kationen, z.B. K+.
Man unterscheidet die Silikate nach
der struktururellen Anordnung der Si-O-Tetraeder (Insel-, Ketten-, Band-,
Schicht-, Gerüststruktur) in:
-
Inselsilikate: Die hier vorliegenden isolierten
[SiO4]4--Tetraeder existieren
als unabhängige Einheiten und werden über weitere Kationen wie
Fe2+, Mg2+ oder
Zr4+ verknüpft. Beispiele für Inselsilikate sind
Olivin (Fe,Mg)2[SiO4], Zirkon
Zr[SiO4], aber auch die Minerale der Granatgruppe wie
Almandin
Fe2+3Al2[SiO4].
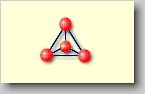 |
| Modellhafte Darstellung der
Inselsilikate |
| (
Quelle: Büro für angewandte Mineralogie, Dr. Stephan Rudolph,
http://www.a-m.de/deutsch/lexikon/mineral/sio4-tetraeder.htm) |
-
Kettensilikate: Kettensilikate bestehen aus aneinander
gereihten Si-Tetraedern mit je einem gemeinsamen O-Ion. Die Ketten sind
untereinander durch 2-wertige Kationen verbunden, die den Ladungsausgleich
bewirken. Die aus Einerketten bestehenden Kettensilikate werden als
 Pyroxene bezeichnet. Ein
Vertreter ist der Pyroxene bezeichnet. Ein
Vertreter ist der  Augit
(teilweise ist Al anstelle Si in den Tetraedern;
Hauptvertreter der Pyroxene in basischen Magmatiten). Werden die
[SiO4]4--Tetraeder zu
unendlichen Ketten verbunden, erhält man Ketten mit der Formel
[SiO3]2-. Augit
(teilweise ist Al anstelle Si in den Tetraedern;
Hauptvertreter der Pyroxene in basischen Magmatiten). Werden die
[SiO4]4--Tetraeder zu
unendlichen Ketten verbunden, erhält man Ketten mit der Formel
[SiO3]2-.
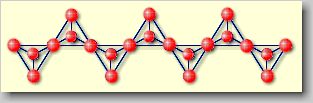 |
| Modellhafte Darstellung der
Kettensilikate |
| (
Quelle: Büro für angewandte Mineralogie, Dr. Stephan Rudolph,
http://www.a-m.de/deutsch/lexikon/mineral/sio4-tetraeder.htm) |
-
Bandsilikate: Bandsilikate bestehen aus Doppelketten, die durch
parallele Anordnung von je 2 Tetraederketten und deren Verbindung über
gemeinsame O-Ionen gebildet werden. Häufig findet ein isomorpher Ersatz des Si
durch Al statt. Die aus Doppelketten aufgebauten Bandsilikate werden auch als
 Amphibole bezeichnet. Ein
wichtiger Vertreter ist die Fe-haltige Amphibole bezeichnet. Ein
wichtiger Vertreter ist die Fe-haltige
 Hornblende, die Bestandteil
von basischen Magmatiten und sehr verwitterungsempfindlich ist. Werden zwei
Ketten über die Tetraederspitzen der Länge nach verbunden, so erhält man
Bandsilikate mit der Formel
[Si4O11]6-.
In der Systematik werden die Bandsilikate meist unter den Kettensilikaten
eingeordnet. Hornblende, die Bestandteil
von basischen Magmatiten und sehr verwitterungsempfindlich ist. Werden zwei
Ketten über die Tetraederspitzen der Länge nach verbunden, so erhält man
Bandsilikate mit der Formel
[Si4O11]6-.
In der Systematik werden die Bandsilikate meist unter den Kettensilikaten
eingeordnet.
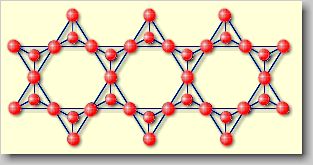 |
| Modellhafte Darstellung der Bandsilikate |
| (
Quelle: Büro für angewandte Mineralogie, Dr. Stephan Rudolph,
http://www.a-m.de/deutsch/lexikon/mineral/sio4-tetraeder.htm) |
-
Schichtsilikate: Werden die vorstehend beschriebenen
[SiO3]2--Ketten zu
unendlichen Schichten zusammengefügt, so erhält man Schichtsilikate mit
[Si2O5]2-.
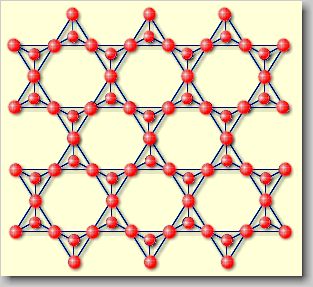 |
| Modellhafte Darstellung der
Schichtsilikate |
| (
Quelle: Büro für angewandte Mineralogie, Dr. Stephan Rudolph,
http://www.a-m.de/deutsch/lexikon/mineral/sio4-tetraeder.htm) |
-
Gerüstsilikate: Gerüst-Silikate bestehen aus dreidimensional
verknüpften SiO4]4--Tetraedern, wobei jedes O-Ion gleichzeitig zwei Tetraedern
angehört (so kommt man zu einem Verhältnis (Si,Al):O=1:2). Es findet ein
teilweiser Ersatz von Si durch Al statt, wobei der Ladungsausgleich durch den
Einbau von 1- und 2-wertigen Kationen erfolgt.
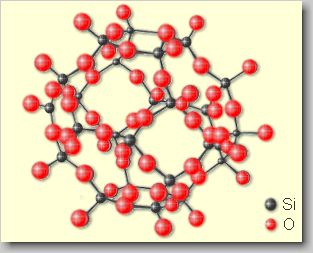 |
| Modellhafte Darstellung der Gerüstsilikate
|
| (
Quelle: Büro für angewandte Mineralogie, Dr. Stephan Rudolph,
http://www.a-m.de/deutsch/lexikon/mineral/sio4-tetraeder.htm) |
Vertreter sind die Feldspäte, die 50% der gesamten Lithosphäre
ausmachen und mit ihrem Gehalt an Basen, Si und Al wichtige
Ausgangsmaterialiender Bodenbildung darstellen, z.B.
 Orthoklas
(Kalifeldspat) und Orthoklas
(Kalifeldspat) und
 Plagioklas sowie die Plagioklas sowie die
 Feldspatvertreter. Feldspatvertreter.
Feldspäte sind als wichtigste Mineralgruppe mit ca. 60% am
Aufbau der Erdkruste beteiligt. Sie lassen sich relativ gut spalten (daher der
Name) und sind Mischungssysteme. Je nach Gehalten an K, Na oder Ca werden sie
in Orthoklase ("gerade spaltend") und Plagioklase ("schief spaltend")
unterteilt. Ein Beispiel für Orthoklas ist der Kalifeldspat
(KalSi3O8) als Hauptgemengeteil
der sauren Magmatite. Der Plagioklas Kalk-Natron-Feldspat besteht aus
Mischkristallen von Albit
(NaAlSi3O8) und Anorthit
(CaAl2Si2O8).
Quarz
Quarz ist eine Mineral aus Siliziumdioxid
(SiO2) aus der Gruppe der Silikate mit Gerüststruktur
mit allseitig verknüpften Si-Tetraedern. Alle Ladungen der
Si4+-Ionen und O2--Ionen sind
ausgeglichen. Quarz ist das zweithäufigste Mineral der Magmatite und
Metamorphite, sowie häufigstes Mineral in Sedimenten. Aufgrund seiner hohen
Verwitterungsstabilität reichert sich Quarz vor allem in Sanden an häufigstes
Bodenmineral an und bildet den überwiegenden Teil des
 Mikroskeletts. Mikroskeletts.
|

 zurück | weiter
zurück | weiter

 zurück | weiter
zurück | weiter